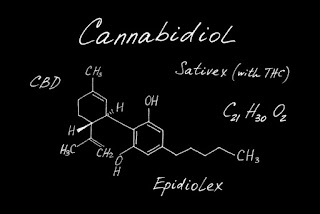
Vào ngày 25 tháng 6 năm 2018, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã công bố phê duyệt lần đầu tiên của một loại thuốc dược phẩm có nguồn gốc từ cần sa. Epidiolex (cannabidiol hay CBD) đã được chấp thuận để điều trị hai rối loạn co giật trẻ em hiếm gặp, hội chứng Lennox-Gastaut và hội chứng Dravet.¹
Vào ngày 27 tháng 9 năm 2018, Cơ quan quản lý thuốc thực thi (DEA) đã công khai đưa thuốc Epidiolex – và sản phẩm thuốc trong tương lai có chứa CBD có nguồn gốc từ cần sa không quá 0,1% THC vào trong Phụ lục V của Đạo luật được kiểm soát (CSA).²
Những sự kiện này biểu thị các mốc lịch sử trong hành trình của Cannabis từ một nguồn hàng dệt và thuốc vào đầu thế kỷ XIX, đến một loại thuốc bất hợp pháp và bây giờ là một loại thuốc được FDA chấp thuận.
Pháp luật phức tạp.
Mặc dù Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đang lập danh mục với loại Epidiolex, vốn là lần đầu tiên DEA thừa nhận rằng cần sa có chứa một “hợp chất an toàn sử dụng trong y tế”, thế nhưng nó đã không thay đổi tình trạng pháp lý của bản thân chất CBD.
Vào ngày 22 tháng 5 năm 2018, DEA đã ban hành một chỉ thị nội bộ cho biết: “Sản phẩm và nguyên liệu được làm từ cây Cannabis và và những sản phẩm nằm ngoài định nghĩa cần sa của CSA (như hạt tiệt trùng, dầu hoặc bánh làm từ hạt, sợi thân cây trưởng thành) sẽ không bị quản lý bởi CSA .¹² Mặc dù những phát biểu này làm rõ rằng CBD, nếu có nguồn gốc từ một nguồn không phải là cần sa thì sẽ không bị kiểm soát, nhưng họ không nói rõ rằng CBD từ cây gai dầu công nghiệp là hợp pháp. Hơn nữa, những nhóm cây này của cần sa lại không phải là nguồn CBD khả thi. Kết quả là, sự nhầm lẫn vẫn là nhầm lẫn.
Luật Nông Nghiệp 2018.
Luật nông nghiệp năm 2018 đã được thông qua vào tháng 12 và chính thức loại cây gai dầu ra khỏi danh sách cấm. Luật này quan niệm cây “cây gai dầu công nghiệp” là tất cả mọi bộ phận của cây Cannabis sativa có hàm lượng THC delta-9 không vượt quá 0,3% khối lượng thô, bao gồm các “chế phẩm”, “chiết xuất” và “cannabinoids”. Quan trọng nhất, bộ luật này đã đưa các sản phẩm CBD phổ biến, như CBD từ gai dầu, ra khỏi sự giám sát của CSA.
Trước khi có đạo luật Nông nghiệp 2018, cây gai dầu trồng trong nước chỉ hợp pháp nội liên bang khi được trồng theo chương trình thí điểm như vậy. Trong năm 2017, tổng số 23,343 mẫu cây gai dầu được trồng trên 19 tiểu bang. Cho tới lúc này, 41 tiểu bang đã thông qua luật để cho phép họ tận dụng các chương trình thí điểm gai dầu theo Luật nông nghiệp năm 2014. Hiện nay, chỉ có một số lượng hạn chế các sản phẩm CBD có mặt ở Mỹ là được sản xuất từ gai dầu nội địa. Điều này sẽ được thay đổi nhanh chóng khi đạo luật Nông nghiệp 2018 thúc đẩy sự phát triển trong lĩnh vực này.
Trước thời kì Epidiolex
Để làm phức tạp hơn nữa, trước khi Epidiolex được chấp thuận, FDA đã tuyên bố rõ ràng rằng “sản phẩm CBD được loại trừ khỏi chế độ bổ sung ăn uống” vì tình trạng pháp lý của CBD đang nằm Chương trình Điều tra Thuốc mới (IND) theo Đạo luật Thực phẩm, Dược phẩm và Mỹ phẩm (FD & C) Act). CBD không còn là thuốc mới điều tra (IND) nữa. Nó được chấp thuận. Kết quả là, CBD không thể được bao gồm trong một chế độ ăn uống bổ sung.
Với sự chấp thuận của FDA về Epidiolex và tuyên bố công khai của FDA rằng các sản phẩm CBD bị loại trừ ra khỏi định nghĩa pháp của một thành phần thực phẩm bổ sung, tương lai của các sản phẩm CBD trực tuyến và không theo toa là không chắc chắn. FDA có thẩm quyền thực thi Đạo luật về Thực phẩm, Thuốc và Mỹ phẩm Liên bang (Đạo luật FD & C) đối với các sản phẩm được làm từ CBD. Cần lưu ý rằng FDA là một cơ quan y tế công cộng với vô số các ưu tiên cạnh tranh và ngân sách thực thi hạn chế. Khi xem xét một hành động thực thi, FDA cân nhắc nhiều yếu tố, bao gồm cả các lợi ích và tác hại. Cho đến nay, các tác hại liên quan đến các sản phẩm CBD có nguồn gốc từ cây gai dầu phần lớn không được ghi lại.
Kết luận
Tác giả:
2. Schedules of Controlled Substances: Placement in Schedule V of Certain FDA-Approved Drugs Containing Cannabidiol; Corresponding Change to Permit Requirements. 2018; https://www.federalregister.gov/documents/2018/09/28/2018-21121/schedule….
3. (ed) RU. Cannabis Inflorescence Monograph: a Monograph. 2014:66, Scotts Valley, CA.
4. Adams R, Hunt M, Clark JH. Structure of Cannabidiol, a Product Isolated from the Marihuana Extract of Minnesota Wild Hemp. I. Journal of the American Chemical Society. 1940;62(1):196-200.
5. Michoulam R, Shvo Y. Hashish. I. The structure of cannabidiol. Tetrahedron. 1963;19(12):2073-2078.
6. U.S. Total CBD Market By Sector (in Millions) – New Frontier. 2018; https://newfrontierdata.com/marijuana-insights/u-s-total-cbd-market-sect….
7. Section 802 – Title 21 United States Code (USC) Controlled Substances Act. 2018; https://www.deadiversion.usdoj.gov/21cfr/21usc/802.htm.
8. Is CBD illegal under the new DEA “marihuana extract” rule? A legal analysis. | Kight on Cannabis. 2018; https://cannabusiness.law/is-cbd-illegal-under-the-new-dea-marihuana-ext….
9. Hudak J, Stenglein C. DEA guidance is clear: Cannabidiol is illegal and always has been. 2017; https://www.brookings.edu/blog/fixgov/2017/02/06/cannabidiol-illegal-and….
10. DEA / Drug Scheduling. 2018; https://www.dea.gov/druginfo/ds.shtml.
11. 21 U.S. Code § 801 – Congressional findings and declarations: controlled substances | US Law | LII / Legal Information Institute. In: @LIICornell; 2018.
12. DEA Internal Directive Regarding the Presence of Cannabinoids in Products and Materials Made from the Cannabis Plant. 2018; https://www.deadiversion.usdoj.gov/schedules/marijuana/dea_internal_dire….
13. hemp | Description & Uses. 2018; https://www.britannica.com/plant/hemp.
14. 7 U.S. Code § 5940 – Legitimacy of industrial hemp research | US Law | LII / Legal Information Institute. In: @LIICornell; 2018.
15. Court USA. Hemp Industries Association v. United States DEA. In: Court UA, ed. LEXIS 11005 9th Circuit; 2018.
16. The Hemp Farming Act of 2018 | Vote Hemp [press release]. @votehemp, 2017-10-31 2017.
17. McConnell M. Text – S.2667 – 115th Congress (2017-2018): Hemp Farming Act of 2018. In:2018.
18. Hemp Industries Association, et al, v. Drug Enforcement Administration, 333 F.3d 1082. In: Circuit t, ed. 9th Circuit 2003.
19. Hemp Industries Association, et al, v. Drug Enforcement Administration, 357 F.3d 1012 In: Circuit t, ed. 9th Circuit 2004.
20. Final Ruling, Hemp Industries Association v. DEA, 357 F.3d 1012. In: Circuit t, ed2004.
21. Legislatures NCoS. State Medical Marijuana Laws. 2018; http://www.ncsl.org/research/health/state-medical-marijuana-laws.aspx.
22. Commissioner Oot. Public Health Focus – FDA and Marijuana: Questions and Answers. [WebContent]. 2018; https://www.fda.gov/NewsEvents/PublicHealthFocus/ucm421168.htm.
23. FDA. FDA Response to Biostratum Citizen Petition, No. FDA-2005-P-0259-0005 In: FDA, ed: FDA; January 12, 2009.
24. Burke FM. Red yeast rice for the treatment of dyslipidemia. Current atherosclerosis reports. 2015;17(4):495.
25. Register F. Administrative Proceeding; Re: Pharmanex, Inc. In: Food and Drug Administration H, ed. Vol Vol. 63. Federal Register Federal Register Tuesday, January 13, 1998.
26. CBD & Hemp Supplement Reviews | ConsumerLab.com. 2018; https://www.consumerlab.com/reviews/cbd-oil-hemp-review/cbd-oil.
27. Bonn-Miller MO, Loflin MJE, Thomas BF, Marcu JP, Hyke T, Vandrey R. Labeling Accuracy of Cannabidiol Extracts Sold Online. Jama. 2017;318(17):1708-1709.
28. Commissioner Oot. Public Health Focus – Warning Letters and Test Results for Cannabidiol-Related Products. [WebContent]. 2018; https://www.fda.gov/newsevents/publichealthfocus/ucm484109.htm.
29. Commissioner Oot. Press Announcements – FDA warns companies marketing unproven products, derived from marijuana, that claim to treat or cure cancer. 2018.
30. Corroon JM, Phillips J. A Cross-Sectional Study of Cannabidiol Users. Cannabis and cannabinoid research. 2018.
Đơn Vị Tài Trợ: